Ligação três centros dois elétrons
Uma ligação três centros dois elétrons ou ligação tricentrada com dois elétrons (3c-2e) é uma ligação química em que um par de elétrons é compartilhado entre três átomos, diferentemente de uma ligação covalente convencional, na qual um par de elétrons é compartilhado entre dois átomos. Consequentemente, a ligação 3c-2e consiste em uma única ligação covalente unindo três átomos. [1] Esta ligação é frequentemente executada por átomos que possuem deficiência de elétrons, sendo que três átomos compartilham dois elétrons entre si. Quando um dos átomos envolvidos é um hidrogênio, ela também é conhecida por ponte de hidrogênio (no Brasil) ou hidrogénio (em Portugal), embora tal expressão também seja aplicada, em sentido menos técnico, às ligações de hidrogênio (que, no entanto, são um tipo de interação completamente diferente).
Descrição[editar | editar código-fonte]
Esse tipo de ligação é bem pouco comum na Natureza e ocorre geralmente em compostos covalentes nos quais alguns dos átomos são deficiente em elétrons, portanto, incapazes de completarem o octeto realizando ligações convencionais. As ligações 3c-2e são particularmente frequentes em compostos de boro (como os boranos), bem como alguns compostos covalentes de berílio, alumínio e alguns metais, além de certos carbocátions não-clássicos como o norbornil.
A combinação de três orbitais atômicos forma três orbitais moleculares: um ligante, um não-ligante e um antiligante. Os dois elétrons vão para o orbital ligante, resultando em um efeito de rede de ligação e constituindo uma ligação química entre os três átomos. Em muitas ligações comuns desse tipo, o orbital ligante é deslocado na direção de dois dos três átomos, em vez de ser igualmente distribuído entre os três. O exemplo mais simples de uma ligação 3c-2e é o hidrogênio protonado molecular, H3+.[2]. Isto resulta numa única ligação covalente unindo simultaneamente três átomos.
Exemplos[editar | editar código-fonte]
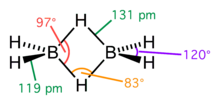
Este tipo de ligação é vista em vários compostos de boro, como o diborano, B2H6; o monômero BH3 é instável já que o átomo de boro possui seis elétrons de valência e, portanto, para formar um octeto estável compartilha elétrons com uma ligação B-H a outro átomo de boro, formando uma ligação B-H-B 3 centros dois elétrons. No diborano, há duas dessas ligações: dois átomos de hidrogênio realizam uma ponte entre os dois átomos de boro, deixando dois átomos de hidrogênio adicionais em ligações B-H ordinárias em cada átomo de boro. Este padrão de ligação é também visto no trimetilalumínio (Al(CH3)3), cuja estrutura real é um dímero (Al2(CH3)6), onde o átomo de carbono de um grupo metil realiza essa ponte.
Nos boranos de estrutura mais complexa, podem existir tanto ligações tricentradas B-H-B quanto ligações B-B-B, formando estruturas semelhantes a gaiolas poliédricas. Nesses clusters, as ligações entre os boros são frequentemente híbridos de ressonância entre ligações covalentes convencionais B-B e ligações 3c-2e B-B-B. Algumas dessas estruturas, como o ânion em forma de gaiola icosaédrica B12H122- e seus derivados, que possuem ligações 3c-2e (juntamente com ligações comuns) apenas entre os boros, são excepcionalmente estáveis devido ao híbrido de ressonância obedecer à regra de Hückel e, portanto, ser considerado um sistema aromático.
Complexos organometálicos como o ferroceno ([Fe(C5H5)2]) e o Sal de Zeise K[PtCl3(C2H4)]•2H2O, também contêm ligações 3c-2e em suas estruturas, resultantes da interação entre uma ligação dupla C=C (no caso, a ligação pi) e o átomo metálico.
Este tipo de ligação ocorre também em alguns compostos de carbono, onde é algumas vezes referida como hiperconjugação; outro nome para ligações três centros dois elétrons assimétricas.
Rearranjos de carbocátions ocorrem através da transição de estado de ligações três centros. Devido às estruturas das ligações três centros possuírem quase a mesma energia que os carbocátions, praticamente não há energia de ativação para esses rearranjos, o que faz com que eles ocorram a taxas extraordinariamente altas.
Várias espécies químicas chamadas de carbocátions não-clássicos possuem ligações três centros dois elétrons entre alguns de seus átomos. Talvez a estrutura desse tipo mais conhecida e estudada seja o cátion norbornil.
Ver também[editar | editar código-fonte]
Referências
- ↑ ATKINS P. W., OVERTON, T.; ROURKE, J.; WELLER, M.; ARMSTRONG, F.A. Química Inorgânica. Porto Alegre: Bookman, 2017. p. 313. link.
- ↑ «IUPAC Gold Book» (PDF) (em inglês)
